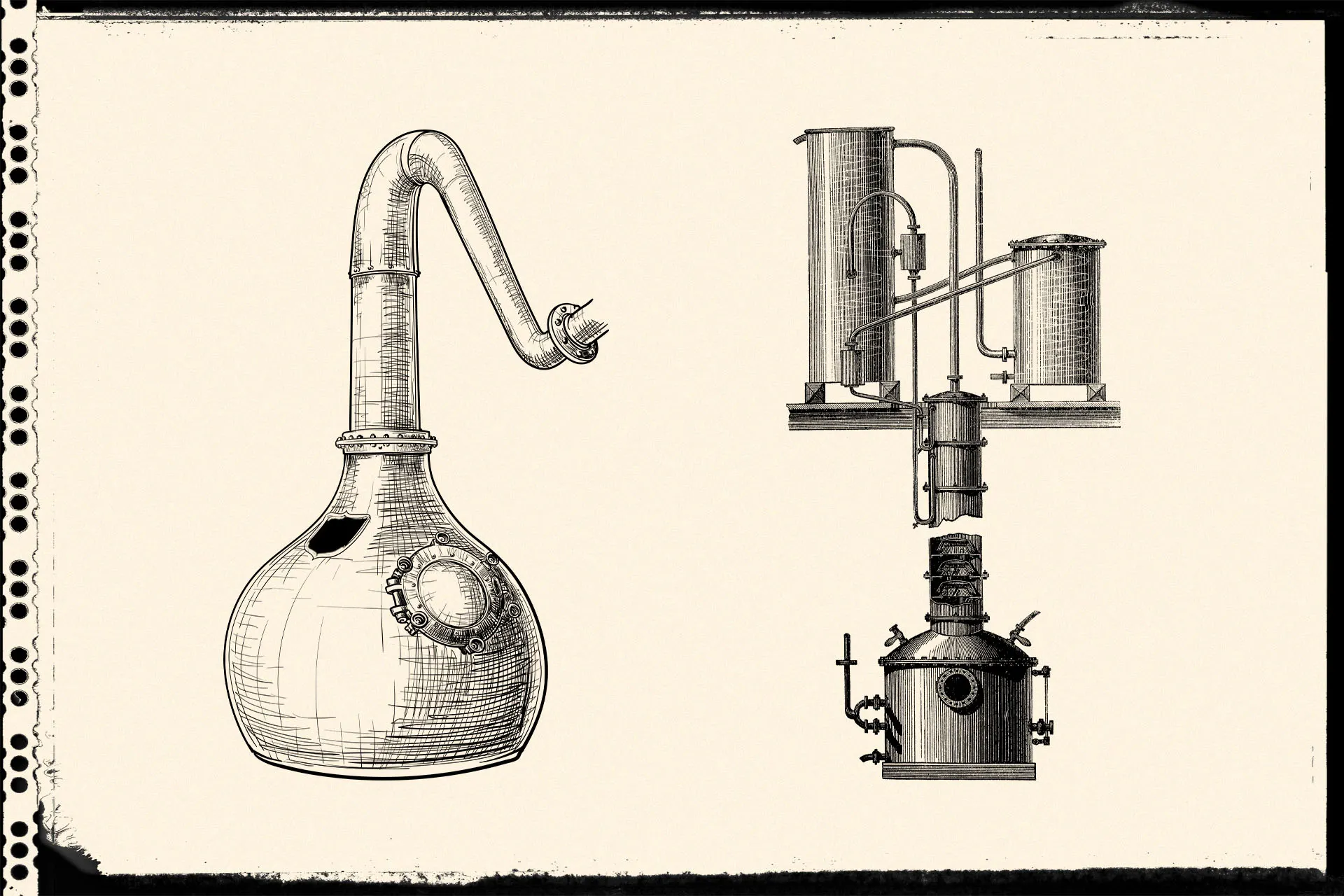
文章中威友们最不熟悉的应该算是第三种设置:柱式批次蒸馏,原因很简单,就是我们熟悉的苏格兰威士忌酒厂没有一间是使用这种蒸馏设置的。Heriot-watt 学校的蒸馏室有一座这种蒸馏器,而这种蒸馏器的优点是不用太高大就可做出酒精度较高的酒,而且速度也快很多。按我的理解这种蒸馏器在苏格兰有两个缺点:(一)若用来蒸馏谷物威士忌的话,不能连续蒸馏会大大增加成本,经济上未必有着数;(二)若用来蒸馏麦芽威士忌的话,应该会被SWA骂说这不算是一种“pot still”,尽管法规上好像没有为何谓pot still作一个清晰的法律定义。
—— Mr. J Whiskiology
在制作苏格兰威士忌时,无论是麦芽威士忌或是谷物威士忌,肯定都少不了”蒸馏”这个步骤。蒸馏几乎可说是制造各式烈酒的最常见方式,因为借由蒸馏可以很容易得将酒精度提升。但是为什么蒸馏可以达到提高酒精度的效果呢?以下将做个简单介绍:
蒸馏是一种将混合物中不同物质分离的方法之一。将某混合液加热后,该混合液会开始沸腾,此时混合液所产生的气体中,较容易挥发的物质比例会较在原混合液中高。将这些气体收集起来再冷却成液体后,这些液体中较容易挥发的物质比例当然就会比在原混合液中高。
举苏格兰麦芽威士忌蒸馏的例子来说,发酵完的酒汁若只观察其中含量最多的两样物质(水与乙醇)并忽略掉其他化合物,可视为单纯将乙醇与水混和的混合液。假设该混合液中乙醇与水的体积比为8%(亦即酒精度为8% abv),拿去在一大气压的情况下做蒸馏时,大约加热至94.5度C时会开始沸腾产生大量气体。若我们将开开始沸腾时产生的这些气体收集并冷凝成蒸馏液,我们会发现这些蒸馏液的酒精浓度大约是45% abv。由于我们从原本8% abv的酒汁中拿走了一些45% abv的成分,所以酒汁的酒精度会稍微下降,接着蒸馏下去所产生的蒸馏液酒精度也会稍微小于45% abv。持续蒸馏时酒汁的温度会逐渐提高,而收得的蒸馏液浓度会逐渐降低,通常来说第一次蒸馏会持续到收得的蒸馏液降到1%左右才停止,此时酒汁中的酒精浓度大概也剩0.1%左右了,继续蒸馏下去有点浪费能源,所以这些剩下的酒汁废液(称为pot ale)会被排出蒸馏器,接着准备进行下一轮蒸馏。
在以上的蒸馏过程中,我们会发现几件事情:
1. 两种不同沸点的物质混合形成的液体,若这混合液中的两物质都可挥发,且A沸点较低(例如乙醇,一大气压时沸点78.4度C),B沸点较高(例如水,一大气压时沸点100度C),则当加热到温度达A的沸点(78.4度C)时,不会发生混合液中A开始蒸发而B完全留在液体中的情况。事实上,该混合物会因两物质的比例不同,导致加热到A的沸点时该混合物还不会沸腾。如上例,酒精度为8% abv的乙醇与水混合液必须加热94.5度C时才会开始沸腾。而当该混合物开始沸腾时,此时产生的气体是A与B混合在一起的气体(上例中冷凝后酒精度是45% abv的气体),且这些气体中A与B的比例会比还未蒸发的液体(酒精度8% abv)中A与B的比例还高,也就是说蒸馏液中A的浓度被提升了。
2. 蒸馏时,容器内的液态混合物会产生蒸气,这些蒸气造成的压力称为蒸气压,温度越高则蒸气压越高,当蒸气压等于大气压力时我们会说混合液开始沸腾了。由于上面的例子中体积比8%的酒精产生的蒸气压跟体积比92%的水在94.5度C左右时合作产生的蒸气压大概是一个大气压力,所以我们说他在94.5度C时会开始沸腾,这个温度点被称为泡点(bubble point),也有人直接叫他沸点(在混合溶液中讲沸点溶液混淆,而且也不知道是在讲哪个物质的沸点,所以我还是习惯称之为泡点)。
3. 理论上我们如果在一大气压下将8% abv的酒汁只简单蒸馏一次,其蒸馏液的酒精度很难超过45% abv(因为A物质的浓度在刚沸腾时的蒸汽中最高,接着会越来越低),若要继续提升只能把这些蒸馏液收集起来再拿去做第二次蒸馏。
上述乙醇与水的例子是用大家比较熟悉的体积浓度来做解释,但由于体积浓度容易随温度而改变,例如在夏天高达35度C的室内把40% abv (通常此数值是在20度C的情况下测得的) 的威士忌拿去用比重计测酒精度时,你会发现测出来的酒精度变成将近45% abv了。所以实际在应用上时会比较常使用莫耳浓度(% mol)而非体积浓度来做计算。
以上的概念若正确的话,接着讨论蒸馏的计算就会比较容易理解了。
蒸馏的原理是利用混合物中各物质在固定温度下,其饱和蒸气压不同而达成的。若在某个温度下A的饱和蒸汽压比B的高,这代表该温度下A会比B容易挥发,也就是A产生的气体较多,因此A气体造成的压力(蒸气压)较大。假设这两种物质可形成理想溶液,且我们在定温定压下某容器中发现A与B的液体莫耳数比为1:1,但是他们产生的气体中莫耳数比是2:1,这样我们会说A的挥发度比B高,而A比B的相对挥发度(relative volatility,通常写作αAB)就是2,也就是说A的挥发能力是B的两倍。那如果这两物质在混合液中的莫耳数比不是1:1的话怎么办呢?
先假设C与D两物质在定温定压时的饱和蒸汽压完全一样,也就是C与D的相对挥发度相同。若这两物质可形成理想溶液,当这两物质以不同莫耳数混合时,我们会发现他们产生的气体莫耳数比会跟他们液体中的莫耳数比相同,也就是说拿3莫耳的C与2莫耳的D混合时,他们产生的气体中C与D的莫耳数比是3:2。从这个例子告诉中可看出来,两相对挥发度相同的物质在气体中的莫耳数比会跟他们在液体中的莫耳数比相同。
那如果是相对挥发度不同的A与B两物质以不同莫耳数形成理想溶液的话,他们在气体中的莫耳数比会如何改变呢?假设A与B的相对挥发度αAB是2,但他们在液体中的莫耳数比是1:4 (也就是1份的A与4份的B),那么因为A的挥发能力是B的两倍,所以A即使在液体中只有1份,它也会产生1*2份的A气体,而B在液体中虽有8份,但他只能产生8*1份的气体,所以此时A与B产生的气体莫耳数比是1*2 : 8*1,也就是1:4。
由上面的例子可知道,我们若想知道两物质在定温定压下的相对挥发度αAB,可以利用
αAB = (A在气相中的莫耳数 / A在液相中的莫耳数) / (B在气相中的莫耳数 / B在液相中的莫耳数)
来求得。
其实只要把(A在气相中的莫耳数 / A在液相中的莫耳数)想成A的挥发能力,这样这个算式就比较容易理解了。
到这边我们可以先暂时下个简单的结论:若A的相对挥发性较高,那么A与B的混合溶液经过蒸馏后产生的蒸气中,A的浓度会比原来高(蒸气中的B浓度当然也就比原来低);留下来未蒸发的液体中因为较多的A被取走,所以这些废液中A的浓度会比原来低(废液中的B浓度当然也就比原来高)。因此我们可以借由蒸馏将挥发能力不同的物质分离。
但这边有两点要注意:
1. 两物质的相对挥发度并非一成不变,而是可能随着两物质在液体中的比例、温度与压力而改变。例如体积比为97.2% abv的乙醇与水混合物会在78.2度C时沸腾,但此时他们的相对挥发度是1,代表该该混合物就算拿去蒸馏,蒸馏出来的气体冷凝后也只会是97.2% abv的乙醇溶液,根本是白做工。
2. 多种物质混合时可能会互相影响。例如酒精溶液(乙醇与水)中若有甲醇,此时甲醇对乙醇的相对挥发度会被酒精度所影响。当蒸馏液酒精度超过40% abv时,该相对挥发度会大于1,而酒精度低于40% abv时该相对挥发度则小于1。这也代表说,当蒸馏液酒精度在40% abv以上时,甲醇会比乙醇还要容易被蒸馏出来,但在酒精度40% abv以下时,甲醇反而变得比较难被蒸馏出来。由此可知,并非在任何状况下沸点低的物质都有较高的相对挥发度,所以蒸馏时单纯靠沸点来推估谁会比较早被蒸馏出来是错误的方法。
实际蒸馏时,使用的设备大概可分成四种:
1.简单蒸馏 (又称差分蒸馏、微分蒸馏,属于批次蒸馏)

这种原理跟苏格兰用于麦芽威士忌蒸馏的壶式蒸馏器差不多,干邑也是用这种类型的设备。该类设备进料时一次只能放一批,这批蒸完再蒸下一批,所以常被称为批次蒸馏。虽然他的名称是简单蒸馏,但由于是批次进料,被蒸馏的液体会越来越少,且液体中挥发度较高的物质其比例也会越来低。由于这种方式会用到微分的概念,计算的时候必须要使用到微积分。
2.骤沸蒸馏 (又称闪蒸、骤馏,属于连续蒸馏)

这种设备比较常用在石油提炼工业。
与第一种不同的是,他在进料时会控制进料的温度与压力,通常使进料维持高温高压。当进料通过减压阀进入蒸馏器主体后,进料会瞬间因压力改变而产生物质相态的改变,如果控制好蒸馏器内的温度与压力,进料可瞬间分离成为液体与气体两相态。这时气态的部分,含有比原进料浓度更高的A物质(相对挥发度高),可从顶部被收集。液态的部分则含有比原进料浓度更低的A物质(也就是B变多了),可从底部收集。
这种蒸馏方式是连续进料的,也就是说进料一被送入后马上变为液气两项排出(收集),只要单位时间内进入蒸馏器的进料量跟排出量相同,便可连续进料,因此是连续蒸馏。此蒸馏方法因为是瞬间达成的,没有随时间改变的问题,所以计算比较简单。
3.有回流的批次蒸馏 (柱式批次蒸馏)

可能常碰苏威的酒友会以为只要看到柱式就是连续蒸馏,其实连不连续跟柱式没有关系。这种柱式蒸馏器也是进一批料后就开始蒸,必须等蒸完后才能蒸下一批。做成柱状式为了要容纳里面水平摆放的板(或盘),混合液经过一层的板就很类似被蒸馏过一次,因此板数越多就类似蒸馏越多次。与简单蒸馏比起来,这种设备一次就可做出酒精度较高的酒。在这种蒸馏方式中,每片板上都会有一定量的液态混合物,当液态混合物的量变多时,就会流到比较下面的板。而两板之间的空间则可容纳气态混合物,当气态的量变多时就会跑到更上层的板中。
假设在由上数来第五片板上面有A与B的混合液,莫耳数比为A:B,且A相对挥发度较高,那在此片板上的空间会产生蒸气,蒸气中A的莫耳浓度会比该板液体中的A莫耳浓度高,这些A莫耳浓度较高气体会上升到第四片板中并与该板的液体混合,接着又会产生A莫耳浓度更高的气体继续往更上层跑,因此顶层A的莫耳浓度极高。至于液体则因一直往下层流,所以越下层液体中B的莫耳浓度会越高。
通常往下层流动的液体量与从最上层离开的气体量(最后会被冷凝成蒸馏液的那些)之比值会被称为回流率(reflux ratio),回流率越高代表往下流的液体比例越高,这个数值在计算中极为重要。跟这种有精馏板的设备比起来,简单蒸馏的设备其回流量算非常少的,壶式蒸馏的设备中的回流主要是靠蒸气在蒸馏器铜壁上的凝结与林恩壁(lyne arm)的角度来回流,但壶式蒸馏的这种回流效率其实不会比在蒸馏器里面加一片精馏板还要来得好。至于这种有回流的批次蒸馏,其计算除了要用到微积分,还会受回流率的影响,所以相对复杂。
4.柱式连续蒸馏

这种的原理与苏格兰谷物威士忌蒸馏器、美波的beer still、雅马邑 alambic相同。它的运作方式有点像把骤沸蒸馏串在一起的感觉,而且它跟上述第3种一样有回流。跟简单蒸馏的设备比起来,这种设备不但可做出较高酒精度的酒,还可以连续一直产出。如同骤沸蒸馏,只要这蒸馏器进料量与排出量相同的话,便可稳定的连续进料。
有人可能觉得上述第3种是不是只要让进料跟排出的量相同就变成第4种了?事实上上述第3种因为底部没有可把极高B浓度的液体排出的装置,所以最底层的液体其B浓度会一直上升,最后也是无法连续蒸馏的。而第4种因为B浓度高的液体也被排走,所以最后整个蒸馏器会维持平衡,可连续进料。
这种蒸馏器的进料位置是可变动的,排出口也可以有很多个。一般在进料板下方(含进料板)的区域被称为汽提段(stripping section),至于上方那段区域则被称为精馏段(rectifying section)。最上方的蒸汽产物经冷凝后会有一部分流回最上层作为回流,最下方的液体废液也可重新煮沸并将煮沸后的蒸气排入上层的塔。这种设备的计算因为是连续的,所以不需用到微积分,只要有回流率就可做运算。不过通常有用精馏板的设备都还要算每个板的效率跟一些其他数值,所以也是麻烦。
Author: lovemoonman 尤爱月